CERN70 : De la physique à la médecine
14 novembre 2024 · View in English

Les technologies développées au CERN pour les accélérateurs et les détecteurs ont trouvé de nombreuses applications dans des domaines autres que la physique des particules, notamment en médecine, où elles servent aussi bien à établir un diagnostic qu’à traiter les patients.
Les scientifiques du CERN contribuent à la recherche médicale depuis près de 60 ans, depuis le début des expériences de radiobiologie, en 1965. Trois ans plus tard, Georges Charpak invente la chambre proportionnelle multifils, un nouveau type de détecteur pour lequel il a reçu le prix Nobel de physique, et qui a été utilisé pour l'imagerie médicale au milieu des années 1970. Le perfectionnement des détecteurs et de l'électronique, et les progrès de la science des matériaux ont permis aux médecins de réduire considérablement la dose de radiation reçue par le patient pendant l'examen, tout en améliorant la qualité de l'image. Autre avancée notable, alors que l’on obtenait en 1977 la première image TEP (tomographie par émission de positons) d'une souris au moyen d’un prototype de caméra à positons, David Townsend développait des algorithmes pour reconstituer les données du détecteur d'Alan Jeavons en s’appuyant sur les expériences de radiobiologie de Marilena Streit-Bianchi. En 1979, David Townsend rejoint l'hôpital cantonal universitaire de Genève, où il participe à la construction, sur la base de la caméra à positons, du premier scanner de tomographie par émission de positons (TEP) de l’hôpital.
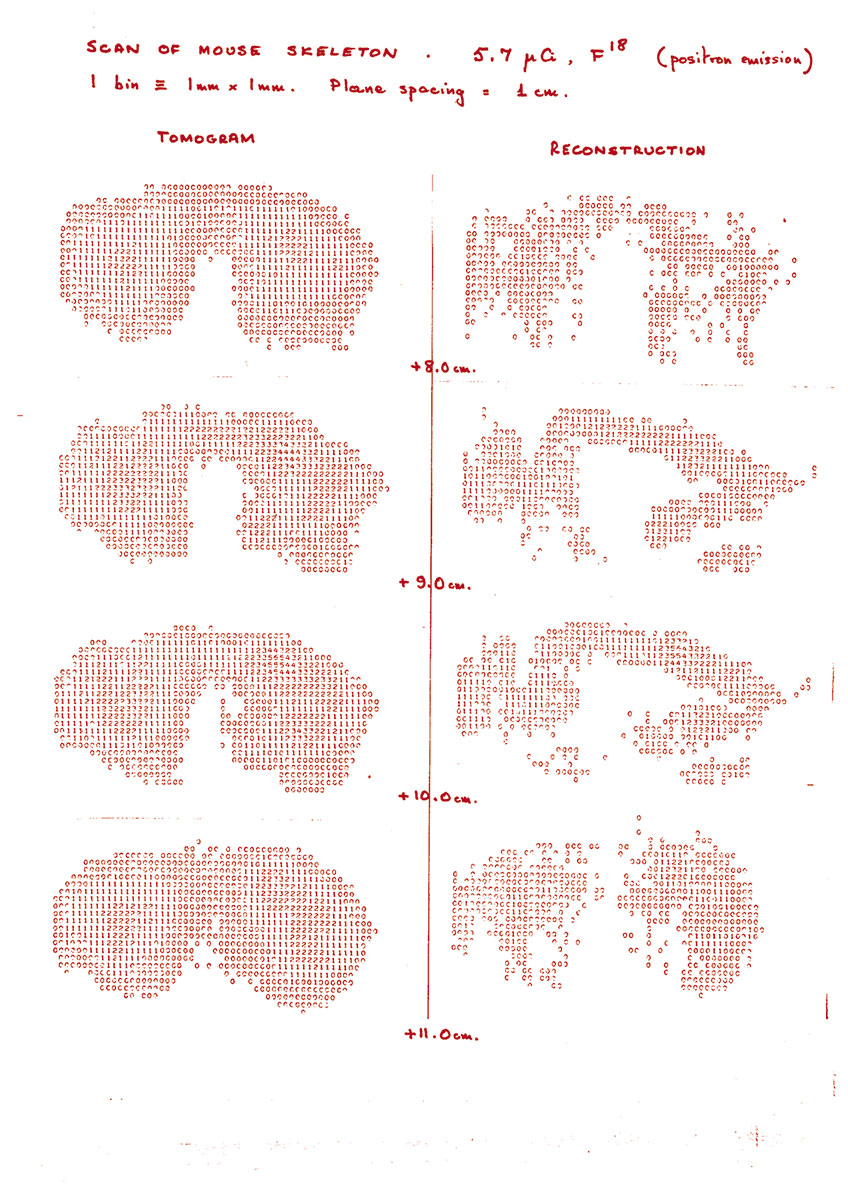
À la même époque, des physiciens du CERN s’intéressent eux aussi à l'utilisation des protons et des ions carbone (noyaux atomiques) pour le traitement du cancer - une idée qui remonte à 1946, lorsque Robert Wilson, physicien américain spécialiste des accélérateurs et futur fondateur et premier directeur du Fermilab, proposa d’utiliser pour la première fois des protons et des ions carbone. Les protons et les noyaux des éléments légers, tels que l'hydrogène et le carbone, conviennent mieux que les rayons X au traitement de certains cancers profonds, car l'énergie déposée (la « dose ») peut être focalisée afin de moins endommager les tissus sains.
À la fin des années 1970 et dans les années 1980, les spécialistes des accélérateurs du CERN étaient de plus en plus consultés pour des projets d'accélérateurs médicaux, en particulier dans le domaine de la thérapie par ions légers, alors en plein essor. Les années 1990 virent le démarrage de la première collaboration Medipix, et de la collaboration Crystal Clear, mise sur pied pour améliorer les cristaux scintillants. Ces collaborations ont toutes deux bénéficié aux détecteurs de particules et à l'imagerie médicale.
Puis, en 1995, Ugo Amaldi, physicien au CERN et père fondateur de la fondation italienne TERA pour la radiothérapie, et Meinhard Regler, du projet MedAustron, réussissent à convaincre la Direction du CERN de lancer l'étude PIMMS (Proton Ion Medical Machine Study), sous la direction de Phil Bryant. Achevée en 2000, la conception développée dans le cadre de l’étude PIMMS a ensuite été adaptée par TERA pour répondre aux besoins du CNAO (Centre national de hadronthérapie oncologique), centre construit en Italie et qui a commencé à soigner des patients en 2011. En 2019, le CERN lança l'étude NIMMS (Next Ion Medical Machine Study) afin de mettre au point des technologies d’accélérateurs de pointe pour une nouvelle génération d'installations de thérapie par les ions plus compactes et moins onéreuses.
Des collaborations en cours avec des médecins, des épidémiologistes et des chercheurs conduisent à des avancées qui contribuent à préserver ou à améliorer la santé de chacun. On peut citer par exemple le rôle de Medipix dans le domaine de l'imagerie médicale, notamment en ce qui concerne les radiographies couleur, la radiothérapie FLASH l'utilisation de radioisotopes pour le diagnostic et le traitement des maladies, l'apprentissage automatique et plus encore.
Témoignage
Lorsque les premiers patients ont été traités au CNAO, j'ai eu le sentiment d'avoir fait des choses très intéressantes en physique, mais mettre au point l’hadronthérapie a été le plus grand accomplissement de ma vie professionnelle.
Ugo Amaldi

Ugo Amaldi était un physicien des particules bien connu au CERN lorsqu'il décida de s’atteler à la création, en Europe, d'un réseau de centres de traitement du cancer utilisant des faisceaux d'ions, en particulier des ions carbone.
« Mon intérêt pour la physique médicale remonte à la fin des années 1950, lorsque j'ai commencé à travailler à l’institut national italien de la santé (Istituto Superiore di Sanità – ISS), à Rome, et que j'ai rédigé un traité de 700 pages, intitulé Fisica delle Radiazioni. J’ai rejoint l’ISS au lieu d'entamer une carrière institutionnelle parce que mon père Edoardo, physicien renommé et l'un des fondateurs du CERN, enseignait à Rome depuis 1937 et que je voulais me démarquer de lui.
À l’ISS, j’ai réalisé des expériences de physique nucléaire et de physique des particules. J’ai travaillé également à temps partiel dans le domaine de la physique des radiations et de la radiothérapie, un sujet qui me plaisait beaucoup. De 1968 à 1973, j’ai dirigé un groupe de physiciens de l’ISS qui travaillaient au CERN. Après une expérience couronnée de succès auprès des anneaux de stockage à intersections (ISR), qui a permis de découvrir que la section efficace proton-proton augmentait avec l’énergie, en 1973, un poste de titulaire m’a été proposé au CERN. De fil en aiguille, en 1981, j’étais devenu le porte-parole de DELPHI, l’une des quatre grandes expériences du LEP (Grand collisionneur électron-positon), que j’avais lancée.
En 1991, après les premiers résultats et un article largement cité sur l’unification supersymétrique des forces fondamentales, DELPHI fonctionnait très bien. Mais je me demandais ce que j’allais pouvoir faire ensuite. J’avais 57 ans, et je savais que je ne mènerais aucune expérience auprès du LHC lorsqu’il serait mis en service. Je souhaitais néanmoins faire quelque chose de nouveau et de directement utile, à la limite de ce qui pouvait être accompli avec les accélérateurs de particules. J’ai donc décidé de revenir à la physique des radiations ; ma femme Clelia me dira plus tard que je suis retourné à mon premier amour.
En fait, l’idée de recourir à la physique pour aider à soigner les gens m’attirait toujours. En 1991, j’ai donc rédigé, avec Giampiero Tosi, physicien médical italien réputé, une proposition pour un centre de traitement du cancer utilisant des faisceaux d’ions carbone (et de protons), un type de traitement que j’ai baptisé peu après « hadronthérapie ». Un an plus tard, avec le soutien de l’Institut italien de physique nucléaire (INFN), nous avons créé la Fondation Tera afin de recueillir des fonds pour financer le personnel travaillant à la conception de ce centre.

À l’époque, tout comme aujourd’hui encore, les cancers étaient essentiellement traités par radiothérapie avec des rayons X. Mais on construisait également des centres spécialisés qui utilisaient des protons. Je me suis intéressé aux résultats obtenus par le Laboratoire Lawrence de Berkeley, aux États-Unis, ainsi qu’aux articles rédigés par Gerhard Kraft, du laboratoire allemand GSI. Environ 1 % des tumeurs traitées aux rayons X s’avèrent résistantes à ces rayons, ainsi qu’aux protons. Il semblait toutefois que ces tumeurs récalcitrantes pourraient réagir si elles étaient bombardées avec des noyaux d’atomes de carbone. Chaque noyau de carbone laisse 20 fois plus d'énergie dans une cellule qu'un proton et provoque ainsi des cassures multiples et irréparables de la double hélice de l'ADN. Les faisceaux de carbone sont donc efficaces pour contrôler les « tumeurs radiorésistantes », telles que les sarcomes des tissus mous, les sarcomes osseux et certains cancers du cerveau, des poumons et des glandes salivaires.
Fin 1995, Meinhard Regler (de MedAustron) et moi avons réussi à susciter l’intérêt de la Direction du CERN pour mettre au point un synchrotron à ions optimisé à des fins d’application médicale. C'est ainsi qu'est née l'étude PIMMS (Proton Ion Medical Machine Study), à laquelle des physiciens et des ingénieurs du CERN, de TERA et du projet MedAustron ont travaillé pendant quatre ans sous la direction de Phil Bryant. Parallèlement, avec TERA, j’ai proposé que le gouvernement italien finance un centre de traitement fondé sur une version améliorée du synchrotron PIMMS, un projet baptisé plus tard PIMMS/TERA. La réalisation de ce centre nécessitant un investissement de plus de 100 millions d’euros, il fut difficile de faire accepter le projet. Mais le gouvernement italien finit par réunir les fonds nécessaires en 2001. En 2003, la Fondation CNAO, avec son équipe de 26 physiciens et ingénieurs, a repris le projet. Sandro Rossi, directeur technique de TERA pendant près de dix ans, est devenu directeur technique, puis directeur général du CNAO. Avec le soutien de l’INFN, la construction du centre a commencé à l’automne 2005, à Pavie, une ancienne ville universitaire proche de Milan. La première irradiation par protons a eu lieu en 2011 et, en 2012, 20 ans exactement après la création de la Fondation TERA, le premier patient a été traité avec un faisceau d'ions carbone.
Lorsque les premiers patients ont été traités au CNAO, j'ai eu le sentiment d'avoir accompli des choses très intéressantes en physique, mais mettre au point l’hadronthérapie a été le plus grand accomplissement de ma vie professionnelle.
Je suis aujourd'hui président émérite du CNAO et je suis fier de voir que le centre continue de se développer. Plus de 5 000 patients ont été traités, 55 % d’entre eux avec des ions carbone ; de plus en plus de patients sont des enfants : en 2023, 62 tumeurs pédiatriques ont été irradiées. En outre, un portique à protons est en cours d'installation et un nouveau système de thérapie par capture de neutrons par le bore sera opérationnel en 2026. Dans l'ensemble, on peut dire que le CNAO, enfant du CERN et de la Fondation TERA, justifie pleinement ma devise : « La physique est belle et utile ».
Découvrez comment les technologies développées pour les accélérateurs de particules, les détecteurs et l’analyse ont trouvé leur place dans les applications médicales.
---
Cette entrevue est tirée en partie de l'ouvrage « Infiniment CERN » publié en 2014 à l'occasion du 50e anniversaire du CERN. La mise à jour a été réalisée en 2024 avec la participation d’Ugo Amaldi.
Ugo Amaldi a été l'un des orateurs lors de la récente conférence publique « De la physique des particules à la médecine », organisée dans le cadre des 70 ans du CERN.
Un nouveau module d'apprentissage numérique sur la TEP est disponible pour les élèves du secondaire. À eux de jouer pour sauver le patient virtuel ! Pour en savoir plus, cliquez ici.
